原子结构 (关于电子阵列)
关于原子核和电子轨道的能量跃迁,我们首先解释一下原子结构(电子排列)。
如下图所示,原子核周围有电子轨道。从内部看,电子轨道有不同类型,称为K壳层、L壳层、M壳层、N壳层等,每个壳层能容纳的最大电子数是固定的。
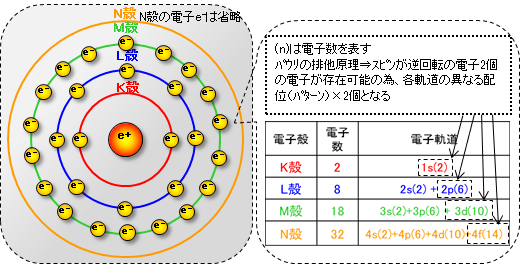
※关于电子轨道,实际上不是图所示的画圆的轨道,而是表示根据量子力学在其位阶水平上电子存在的概率高的云状的东西,不能确定电子本身的位置。
关于电子轨道
除电子壳外,还有几种电子轨道形状不同的图案。这是电子以原子核为中心运动的轨道(对齐,分布),被称为电子轨道,如上图所示被划分为几个轨道。(薛定谔波动方程)
s 轨道;
每个电子壳层中存在一个 s 轨道,其中电子以原子核为中心呈球形分布(1s、2s、3s...),即使一个 s 轨道总共最多有两个电子。电子可以沿相反方向旋转。 (泡利不相容定律)
p 轨道;
L壳层后存在X、Y、Z轴方向的三个配位轨道(2p、3p……),围绕原子核呈8字形(葫芦形)分布,包括反向旋转。电子数,最多可以存在 6 个电子。